Innovación
Investigadores israelíes ayudan a niños con síndrome de Dravet gracias a una innovadora terapia génica
La esperanza media de vida de los niños con este síndrome suele ser corta, con un 10-20% de posibilidades de morir por muerte súbita inesperada en epilepsia antes de los 10 años.

Agencia AJN.- El síndrome de Dravet (SD) es una encefalopatía epiléptica genética poco frecuente que da lugar a crisis que no responden bien a la medicación anticonvulsiva. Comienza en el primer año de vida de un lactante o niño pequeño sano y puede incluir un espectro de síntomas que van de leves a graves.
La esperanza de vida media de los jóvenes con este síndrome suele ser corta, y entre el 10% y el 20% fallecen por muerte súbita inesperada en epilepsia (SUDEP) antes de los 10 años.
El síndrome es una forma grave de epilepsia caracterizada por convulsiones frecuentes y prolongadas (que comienzan antes de los 15 meses de edad) en ocasiones desencadenadas por una temperatura corporal elevada (hipertermia), retraso del desarrollo, trastornos del habla, ataxia, hipotonía, trastornos del sueño y otros problemas de salud. Está causada por una mutación genética en el gen SCN1A, que cuando es normal es necesario para el correcto funcionamiento de las células cerebrales.
El síndrome debe su nombre a la epileptóloga y psiquiatra pediátrica francesa Charlotte Dravet, que ya es octogenaria, quien tuvo la oportunidad de acompañar y observar a pacientes ingresados durante muchos años, lo que dio lugar a algunas de sus principales contribuciones a la epileptología.
Hay esperanza
Pero hay esperanza. Investigadores de la Universidad de Tel Aviv (TAU), entre otras instituciones, desarrollaron una innovadora terapia génica en ratones de laboratorio que podría llegar a ayudar a los niños que padecen SD, que es el resultado de una mutación y no se hereda de los padres, sino que se produce aleatoriamente en el feto.
Los investigadores publicaron sus hallazgos en el Journal of Clinical Investigation con el título «La expresión de NaV1.1 mediada por vectores virales, tras el inicio de las convulsiones, reduce la epilepsia en ratones con síndrome de Dravet».
Los niños con SD presentan inicialmente convulsiones focales confinadas en una zona del cerebro o generalizadas en todo el cerebro. Estas crisis iniciales suelen ser prolongadas y afectar a la mitad del cuerpo, y pueden ir seguidas de crisis que se desplazan al otro lado del cuerpo. A partir del año de edad aparecen otros tipos de crisis que pueden ser muy variadas. El estado epiléptico -un estado de convulsión continua que requiere atención médica de urgencia- puede darse con frecuencia, sobre todo antes de los cinco años.
Como los niños con SD suelen tener un desarrollo normal en los primeros años de vida, después aumentan sus crisis y se ralentiza el ritmo de adquisición de habilidades, por lo que los afectados empiezan a retrasarse en su desarrollo con respecto a sus compañeros. Otros síntomas pueden aparecer a lo largo de la infancia, con cambios en la alimentación, el apetito y el equilibrio.
La Dra. Moran Rubinstein, que dirigió el equipo, declaró que «el SD, cuya incidencia es de aproximadamente uno de cada 16.000 nacimientos, se considera relativamente común entre las enfermedades genéticas raras. A día de hoy, hay unos 70 niños israelíes que la padecen. La enfermedad no es característica de un determinado segmento de la población, no puede predecirse de antemano ni descubrirse durante el embarazo».
Las crisis del SD son difíciles de controlar, pero pueden reducirse con fármacos anticonvulsivantes como la oxcarbazepina, la carbamazepina, la fenitoína y la lamotrigina, aunque no deben utilizarse a diario porque pueden empeorar las crisis. También puede ser útil una dieta cetogénica rica en grasas y baja en carbohidratos. La Administración de Alimentos y Medicamentos de EE.UU. (FDA) aprobó la fenfluramina y el cannabidiol para tratar las convulsiones con SD en niños después de su segundo cumpleaños.
Las terapias genéticas desarrolladas recientemente demostraron su eficacia en ratones con SD, y algunas de ellas incluso se encuentran ahora en fase de ensayos clínicos en humanos. Sin embargo, estos tratamientos demostraron su eficacia en ratones con SD sólo cuando se administran en fases muy tempranas, incluso antes de la aparición de los síntomas. Dado que la terapia génica es un procedimiento complejo e invasivo, no se administra a niños sin un diagnóstico claro de SD.
«Por eso, en este estudio se concentraron en desarrollar un tratamiento que fuera eficaz tras la aparición de las convulsiones, incluso a una edad relativamente tardía. Además, como el síndrome también incluye retrasos en el desarrollo, buscamos desarrollar un tratamiento que aliviara tanto la epilepsia como los síntomas cognitivos», explicó Rubinstein.

Foto de la Dra. Moran Rubinstein (crédito: UNIVERSIDAD DE TEL AVIV)
En las terapias genéticas, los virus suelen utilizarse como portadores que transportan material genético normal al organismo del paciente para que se añada al ADN dañado y permita una actividad normal, continuó Rubinstein.
«Para eso, se manipula el virus; se elimina su material genético original para que no pueda causar enfermedades ni replicarse, y en su lugar se introduce el gen normal correspondiente. En el caso de la SD, como el gen SCN1A es muy grande, no era posible utilizar los virus comunes que suelen emplearse para este fin y se necesitaba un virus capaz de portar y transferir genes grandes. En nuestro estudio, resolvimos este problema utilizando un virus llamado adenovirus canino de tipo 2 como portador del gen normal», agregó el doctor a cargo del equipo.
A continuación, los investigadores inyectaron el virus portador directamente en el cerebro de los ratones con SD para que infectara las células nerviosas disfuncionantes. Los investigadores señalaron que el tratamiento requiere la inyección directa en el cerebro porque el tamaño y las propiedades del virus no permiten atravesar la barrera hematoencefálica.
Se trató a 31 ratones a las tres semanas de edad, tras la aparición de convulsiones espontáneas (equivalente a uno o dos años de edad en niños), y a 13 ratones a las cinco semanas de edad (equivalente a seis u ocho años de edad en niños). La inyección se realizó en varias zonas del cerebro, y además se inyectó un virus vacío en el cerebro de 48 ratones como control.
La mayor eficacia se observó cuando el tratamiento se inyectó a las tres semanas de edad. En estos ratones, las convulsiones cesaron por completo a las 60 horas de la inyección, la esperanza de vida aumentó significativamente y el deterioro cognitivo se reparó por completo. Incluso en los ratones tratados a las cinco semanas de edad se observó una mejora significativa en forma de disminución de la actividad epiléptica y protección frente a las crisis inducidas térmicamente.
En los ratones del grupo de control que recibieron un virus vacío, no se observó ninguna mejoría y padecieron los síntomas de la enfermedad igual que los ratones no tratados; cerca del 50% de ellos murieron prematuramente a consecuencia de la epilepsia grave. El tratamiento se aplicó a ratones sanos sin resultados perjudiciales, lo que constituyó una prueba de su seguridad.
Cuando se inyectó un virus portador de un gen SCN1A normal en el cerebro de ratones con SD, el tratamiento resultó eficaz en diversos aspectos críticos, como la mejora de la epilepsia, la protección frente a la muerte prematura y una mejora significativa de las capacidades cognitivas. Y lo que es más importante, este tratamiento fue eficaz después de la aparición de la epilepsia grave del SD.
«Nuestro tratamiento añadió un gen normal a las neuronas dañadas del cerebro, lo que bastó para restablecer su funcionamiento normal. El retorno del gen normal en su totalidad es especialmente importante para tratar el SD porque en distintos niños la mutación se produce en lugares diferentes del gen y la inyección de un gen completo es un tratamiento uniforme adecuado para todos los pacientes con SD», afirmó el equipo de la TAU a The Jerusalem Post.
Los investigadores también destacaron que descubrieron «que el virus elegido para el estudio infecta muchas células nerviosas del cerebro y se propaga ampliamente más allá del lugar de la inyección, lo que aumenta su eficacia».
«Esperamos que la técnica que desarrollamos en el laboratorio llegue también a la clínica en el futuro y ayude a los niños con esta grave enfermedad. Además, dado que existe una similitud entre Dravet y otras epilepsias raras del desarrollo en cuanto a los síntomas del paciente y los cambios cerebrales, esperamos que este tratamiento también pueda ayudar a otros tipos de epilepsias genéticas, y creemos que las herramientas que desarrollamos en esta investigación allanarán el camino para el desarrollo de tratamientos similares para otras enfermedades raras», expresaron los investigadores.
La investigación se llevó a cabo bajo la dirección de Rubinstein y la estudiante de posgrado Saja Fadila, junto con Anat Mavashov, Marina Brusel y Karen Anderson, todos ellos de la Facultad de Medicina y la Escuela Sagol de Neurociencia de la Universidad de Tel Aviv, y el Dr. Eric Kremer, de la Universidad de Montpellier (Francia). También participaron en el estudio Bertrand Beucher e Iria González-Dopeso Reyes, de Montpellier, y otros investigadores de Francia, Estados Unidos y España.
Los investigadores mencionaron que «hoy en día es habitual realizar un análisis genético a los niños que sufren convulsiones complejas de origen térmico en torno a los seis meses de edad. Pero aunque el análisis detecte que el problema está en el gen SCN1A, el diagnóstico definitivo suele darse después de que la epilepsia empeore, con la aparición de convulsiones espontáneas graves y retrasos en el desarrollo. Aunque es importante tener un diagnóstico precoz, éste suele retrasarse, y la mayoría de los niños no son diagnosticados hasta la edad de uno o dos años, y a veces incluso más tarde».
Rubinstein concluyó que «el tratamiento que desarrollamos es el primero que demostró su eficacia para el SD cuando se administra tras la aparición de convulsiones espontáneas, y el primero que produjo una mejora de la función cognitiva de los ratones con SD. Registramos una patente y esperamos que en el futuro el tratamiento llegue a la clínica y ayude a los niños que lo padecen. Actualmente estamos investigando si también puede servir para otras enfermedades genéticas del neurodesarrollo. La plataforma que desarrollamos es una plataforma para terapias genéticas, y quizá en el futuro podamos empaquetar en el virus portador distintos tipos de material genético normal para tratar otras enfermedades».
Innovación
Científicos israelíes desarrollan tratamiento experimental que mejora la supervivencia en casos de hemorragias graves
Agencia AJN.- Un nuevo tratamiento desarrollado por investigadores de la Universidad Hebrea de Jerusalem en conjunto con el Cuerpo Médico de las Fuerzas de Defensa de Israel (FDI) podría transformar por completo la atención médica de emergencia en situaciones de trauma severo, tanto en el ámbito militar como civil.
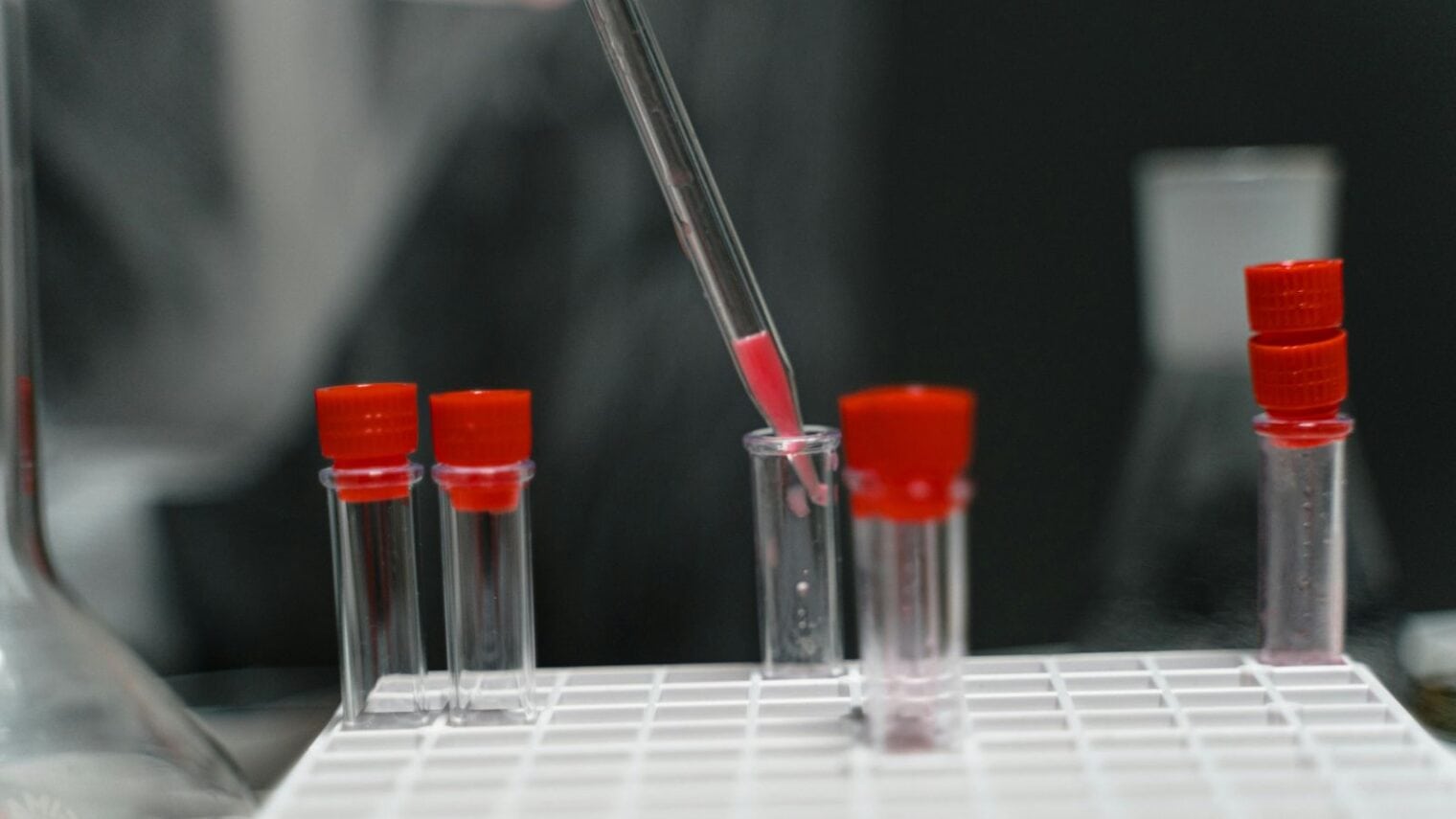
La investigación, publicada recientemente en la revista Scientific Reports, demostró que la activación de una proteína específica —conocida como PKC-ε (Proteína Quinasa C épsilon)— después del inicio de una hemorragia masiva puede triplicar las tasas de supervivencia.
El estudio, liderado por los doctores Ariel Furer y Maya Simchoni del Instituto de Investigación en Medicina Militar (proyecto conjunto entre la Universidad Hebrea y el Cuerpo Médico de las FDI), simuló un shock hemorrágico extrayendo el 35% del volumen sanguíneo de modelos animales. Al aplicar el tratamiento apenas cinco minutos después del inicio de la hemorragia, la supervivencia saltó de un 25% a un 73%.
La clave del tratamiento es que ayuda a estabilizar las funciones cardiovasculares: mantiene la presión arterial, el ritmo cardíaco y la capacidad del corazón para bombear sangre. Además, se observó una mejora en la función mitocondrial del tejido cardíaco, es decir, ayuda a que las células generen energía suficiente para resistir el daño y mantener los órganos funcionando.
“Las hemorragias masivas siguen siendo uno de los mayores desafíos en la medicina de emergencia, tanto en el campo de batalla como en accidentes civiles”, explicó Furer. “Este avance abre una nueva puerta para tratamientos que podrían cambiar radicalmente las tasas de supervivencia en situaciones críticas.”
Actualmente, el tratamiento estándar para este tipo de emergencias es la reposición de fluidos, pero este método muchas veces genera complicaciones adicionales y daños en los tejidos. El enfoque israelí con PKC-ε parece no sólo estabilizar al paciente, sino además proteger los órganos contra ese tipo de daño secundario.
A pesar de los resultados alentadores, los investigadores subrayaron que es necesario avanzar hacia ensayos clínicos para confirmar su efectividad en humanos. Sin embargo, el potencial es enorme, sobre todo para el uso por parte de equipos de primeros auxilios y médicos en zonas de combate o en escenarios de catástrofes.
Con este desarrollo, Israel vuelve a posicionarse a la vanguardia de la medicina de emergencia, aportando conocimiento y soluciones que podrían salvar miles de vidas en todo el mundo.
Fuente: Israel21.
Ciencia
Científicos israelíes: Modelos generales de inteligencia artificial son mejores que los específicos para médicos para diagnosticar casos complejos

Agencia AJN.- Un equipo de investigadores de la Universidad Ben-Gurión del Néguev ha desarrollado una nueva base de datos para evaluar la capacidad de los modelos de propósito general de inteligencia artificial (IA) para diagnosticar casos médicos complejos, según The Press Service of Israel (TPS-IL).
Sus hallazgos, presentados ante la Asociación para el Avance de la Inteligencia Artificial en Filadelfia, sugieren que modelos como el GPT-4o podrían ser más efectivos que los diseñados específicamente para la medicina.
Tradicionalmente, los modelos de propósito general de IA se han probado en casos médicos más simples, como preguntas de exámenes o enfermedades comunes, pero no en los casos complejos del mundo real que los médicos suelen enfrentar. Para subsanar esa deficiencia, los investigadores crearon una base de datos de 3.562 informes de casos médicos del BMC Journal of Medical Case Reports, que incluye descripciones detalladas de casos médicos inusuales y sus diagnósticos. Los casos se presentaron mediante preguntas abiertas y de opción múltiple, simulando escenarios de diagnóstico reales.
Los resultados fueron sorprendentes: GPT-4o superó a modelos médicos como Meditron-70B y MedLM-Large en el diagnóstico de esos casos complejos. GPT-4o logró una precisión del 87,9% en preguntas de opción múltiple y del 76,4% en preguntas abiertas, superando a los especializados.
“Nos sorprendió ver que los modelos generales, como GPT-4o, tuvieran un mejor rendimiento que los adaptados para la medicina. Mostramos que los modelos de lenguaje de gran tamaño pueden utilizarse para diagnosticar casos médicos complejos”, afirmó Ofir Ben-Shoham, uno de los investigadores.
La base de datos CUPCase que creó el equipo podría convertirse en una herramienta valiosa para probar nuevos modelos de IA en el futuro. Está abierta al público y puede ampliarse con casos adicionales a medida que se desarrollen nuevos modelos.
“El objetivo era crear un sistema que pudiera evaluar la eficacia de los modelos lingüísticos para diagnosticar casos complejos del mundo real, no solo los comunes”, afirmó el estudiante de doctorado Uriel Peretz.
El doctor Nadav Rapoport, otro miembro del equipo de investigación, explicó que diagnosticar casos complejos puede ser un proceso largo e incierto, lo que genera retrasos y mayores costos para los pacientes. La base de datos CUPCase, al proporcionar casos reales detallados, puede ayudar a acelerar ese proceso y mejorar la atención del paciente.
La investigación tiene diversas aplicaciones prácticas en el ámbito sanitario, principalmente al mejorar la velocidad y precisión de los diagnósticos médicos.
Modelos de IA como GPT-4o podrían ayudar a los médicos a diagnosticar casos médicos complejos con mayor rapidez, reduciendo los retrasos en el diagnóstico y mejorando los resultados de los pacientes.
La base de datos CUPCase, que incluye una colección de casos del mundo real, puede servir como una valiosa herramienta de apoyo a la toma de decisiones clínicas, ayudando a los médicos a tomar decisiones más precisas, especialmente en casos difíciles o poco frecuentes.
Además, el modelo de IA podría facilitar la formación de profesionales médicos, ofreciendo un recurso interactivo para el aprendizaje de procesos diagnósticos complejos.
Las herramientas basadas en IA también podrían ampliar el acceso a apoyo diagnóstico de expertos en zonas desatendidas, donde los especialistas pueden ser limitados. En entornos de cuidados críticos, los modelos de IA podrían proporcionar asistencia diagnóstica en tiempo real.
-

 Israelhace 12 horas
Israelhace 12 horasIsrael: 17 heridos, dos de ellos graves, tras impacto de misil balístico iraní en Haifa
-

 Medio Orientehace 12 horas
Medio Orientehace 12 horasEliminado en el sur del Líbano el comandante de artillería de Hezbollah responsable de ataques contra Naharía y Haifa
-

 Israelhace 7 horas
Israelhace 7 horasEl jefe de las FDI insinúa una guerra prolongada: «Lanzamos esta campaña para eliminar la amenaza»
-

 Israelhace 14 horas
Israelhace 14 horasNetanyahu y el jefe del Estado Mayor de las IDF se reúnen con altos funcionarios de EE. UU. mientras Trump evalúa atacar Irán
-

 Medio Orientehace 13 horas
Medio Orientehace 13 horasInforme: Ataque con drones en Teherán habría tenido como objetivo a científico iraní especializado en armamento
-

 Guerrahace 21 horas
Guerrahace 21 horasIrán. Israel ataca instalaciones militares y un centro de investigación nuclear en Teherán
-

 Israelhace 14 horas
Israelhace 14 horasLa aerolínea israelí El Al ofrece a sus clientes la opción de regresar a Israel desde Chipre en crucero
-

 Guerrahace 21 horas
Guerrahace 21 horasUn misil iraní impacta en Beer Sheba y causa graves daños











 Suscribite al Whatsapp!
Suscribite al Whatsapp!